早在2月4日,吉利德的2843箱瑞德西韦药物就已经运抵北京,时至今日人们却听到了入组患者太少的消息,“人民的希望”被浇了一头冷水。
瑞德西韦是被世界卫生组织认为是目前唯一可能抗击新冠病毒的药物。“人民的希望”是网友对瑞德西韦英文名 Remdesivir的谐音,也表达了民众对此药的期待。
2月24日的新闻发布会上,世界卫生组织总干事高级顾问布鲁斯·艾尔沃德(Bruce Aylward)透露,瑞德西韦临床试验牵头人、中日友好医院曹彬说其项目现在招募病人变难了,不仅是因为病例减少了,同时诸多没有太大希望的其他研究挤兑了试验资源。
2月15日科技部生物中心主任张新民称,共有168例重症病人和17例轻症病人正在进行瑞德西韦的临床试验。该研究的设计方案中,研究将在武汉金银潭医院等多家接诊的新型冠状病毒感染肺炎患者中进行,首批拟入组病例共计761例,其中包括,轻、中症组患者308例,重症组患者453例。
最有希望的新冠病毒药物临床研究,入组者远未能满足需求。反观另一面则是熙熙攘攘的热闹局面:从1月23日到2月27日,在中国临床试验注册中心新型冠状病毒肺炎临床研究索引中已经有271个结果。
蜂拥而至的众多临床研究抢走了瑞德西韦临床试验大量的患者资源。艾尔沃德呼吁,应该优先那些可能更有希望的研究项目。
DeepTech经多方了解发现,瑞德西韦试验的高门槛、众多临床试验挤兑是瑞德西韦的困境所在。那么瑞德西韦研究结局会是怎样呢?
入组门槛高

以瑞德西韦的重症新冠肺炎临床试验方案为例。试验开始时间为2020年2月6日,研究完成时间为2020年5月1日。这是一项随机、双盲、安慰剂对照的多中心 III期临床试验。
试验方案分为实验组和对照组。实验组患者入组第1天给予瑞德西韦200毫克负荷剂量,之后每天静脉注射100毫克,持续治疗9天;对照组患者入组第1天给予安慰剂200毫克,之后每天静脉注射100毫克,持续治疗9天。
入组的标准有7项,其中一项就会排除掉一部分患者,即核酸检测新冠病毒阳性。因为出于实验室检测缺陷等多种原因,一部分患者多次进行核酸检测阴性,但新冠肺炎症状严重。
入组标准中的另一个门槛是距离发病时间小于12天。事实上,很多医院里的住院患者是不在这个时间窗口中,那么也就无法满足这个要求。
入组方案要求患者在筛查评估之前的30天内没有接受过任何针对新冠病毒的试验性治疗。这个要求让很多患者止步,因为此前有官方或新闻报道推荐某些药物如双黄连口服液,他们可能已经服用过。要知道,这些药物的服用会增加临床研究的不确定因素。
武汉大学人民医院一位人士表示,除了上述障碍,还有患者自身意愿的问题,一些患者不同意入组进行试验。
官方信息显示,2月6日,首个入组的新冠肺炎患者开始用药,目前还不清楚这位68岁的患者是作为试验的一部分还是为了救急。10天后只成功招募了不到200人。目前招募到的人数尚不明确。
不过,瑞德西韦研究还是有了新的希望。2月27日,吉利德科学宣布发起2项针对瑞德西韦治疗新型冠状病毒肺炎的临床试验,全球招募1000人。其中1项随机、对照双盲临床试验已在美国内布拉斯加大学医学中心开展。首位入组患者是1名从“钻石公主”号邮轮撤回的美国人。其试验方案与中国方案略有不同。
紧迫的药物实验却因为缺乏合适的患者而速度放缓,这是在疫情期间快速开发药物的重大挑战。中国的新增感染人数逐渐减少,留给瑞德西韦的时间还有多少?
患者资源遭遇挤兑
蜂拥而至的众多临床研究抢走了瑞德西韦临床试验大量的患者资源。艾尔沃德呼吁,应该优先那些可能更有希望的研究项目。
DeepTech经多方了解发现,瑞德西韦试验的高门槛、众多临床试验挤兑是瑞德西韦的困境所在。那么瑞德西韦研究结局会是怎样呢?
患者资源遭遇挤兑
在中国临床试验注册中心(http://www.chictr.org.cn/)注册的271个新冠病毒研究项目中,包括了治疗性临床试验、诊断试验、干预性研究、观察性研究、流行病学研究。
271个注册新冠肺炎的临床试验中,既有洛匹那韦/利托那韦这样抗艾滋药物研究,也有脐血间充质干细胞的研究、恢复期血浆治疗的研究、维生素 D对患者预后的研究、连花清瘟胶囊中成药研究、甘草酸二胺的研究,甚至还有太极拳对患者康复的研究,有健身气功养肺方对患者功能恢复和生活质量的影响研究,有大豆水提物(豆浆)的临床治疗研究。当然还有众所周知的双黄连口服液研究。
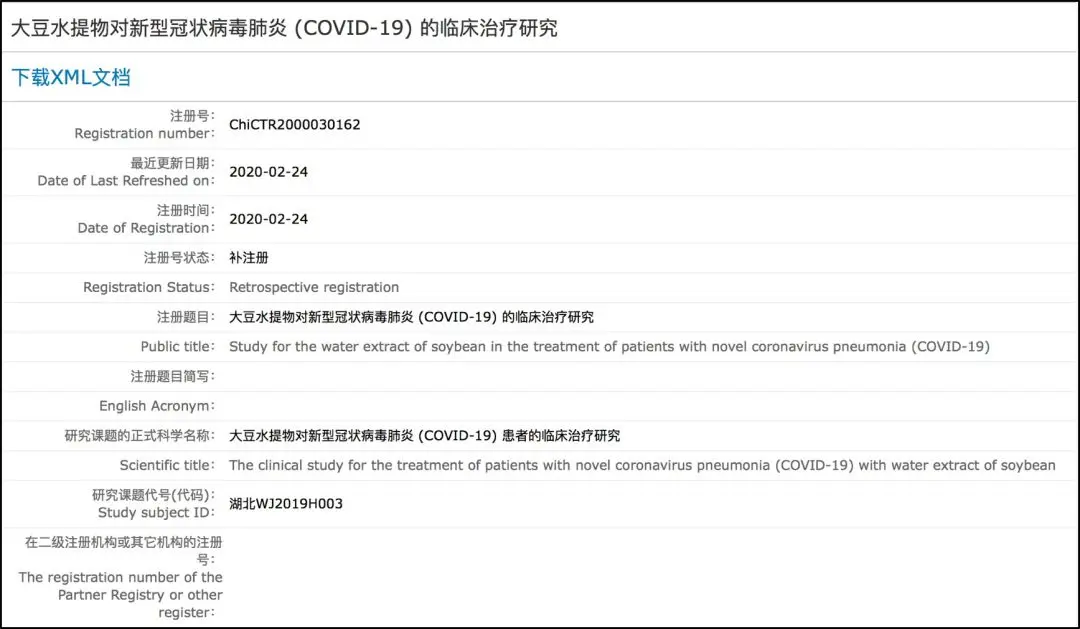
图|喝豆浆治疗新冠肺炎的临床研究
DeepTech了解到,在武汉大学人民医院一个科室的20多名新冠患者中,就参与了多达7个临床试验项目。据介绍,该科室的瑞德西韦项目入组患者仅有2名。
中国临床试验注册中心查询可知,武汉大学人民医院正在进行的项目至少有9个。包括连花清瘟胶囊/颗粒治疗试验2项(针对疑似病例的1项和针对确诊病例的1项),羟氯喹治疗疗效研究,雾化吸入喜炎平注射液治疗研究,评价羟氯喹对新冠暴露后的密切接触者预防效果的研究,医务工作者新冠肺炎易感因素调查与院内防控策略研究,多脏器超声特征性改变,来氟米特临床试验。最近的一个项目是重组人白介素2治疗新型冠状病毒肺炎的临床研究,该项目注册时间是2月24日。中国临床试验注册中心网站显示,该研究尚未获得伦理委员会批准。
业内人士反馈是强烈的。2月24日,《中华流行病学杂志》发表一批卫生统计学与流行病学工作者撰写的《关于科学、规范、有序地开展新型冠状病毒肺炎相关临床试验的建议》提出,除非认为是十分重要的研究,否则需要谨慎。因为目前是病例积压最多、临床最困难的时候,是降低病死率、提高治愈率的关键时刻,要尽量避免对临床救治的干扰,避免增加临床工作的负担。
这篇文章通讯作者系中山大学郝元涛、广州市妇女儿童医疗中心唐金陵、复旦大学姜庆五和北京大学李立明。他们指出,项目众多,而患者数量已经不能满足研究要求,这会导致研究难以获得预期结论。如果样本量不足,对照组的选择不合理,临床研究就难以提供高质量的有效性和安全性证据,使得受试患者、研究者和管理部门的努力付诸东流。
有专家质疑说,很多临床医生不是专门从事研究的,他们在抗疫第一线有多少时间来真正做这研究?
如果这种情况持续下去,那些拥有最多的病人的机构可能最终得到的是糟糕的临床研究结果,因为有能力无条件的人无法进行研究,有条件能力不足的人却将患者资源据为己有。
曹彬怎么办?
如果不能满足当初的试验设计会怎样?曹彬没有回应我们的采访请求。
不少业内看法认为,非常时期无需减持这么严谨、操作上也有困难的设计,可以考虑在样本量和试验设计上作些让步。有多位学者为瑞德西韦项目给出建议,可以考虑放宽招募标准,增加招募中心,延长招募时间。对于前者,可以考虑不仅限于发病时间在12天以内的要求,而是放宽到更长时间。对于后者,可以增加方舱医院作为轻、中度病人的招募中心,还可以考虑增加武汉之外地区的患者。
但前述《中华流行病学杂志》文章不认可对临床研究进行调整的做法,“这些想法也许初衷是好的,但后果往往是得不出可靠的结论,也就是对患者不负责任”。
药智网联合创始人李天泉对 DeepTech表示,既然临床试验方案确定了,原则上是应该严格按照注册方案来进行的,方案要调整可能会带来很多麻烦,比如合作医院的前期培训要增加等等。
李天泉建议,可以考虑采取行政手段,优先保证那些更有潜力的临床研究入组。
当然最好的一个结果是,如果瑞德西韦疗效显著,那么较小样本也能有说服力。不过鉴于新冠肺炎是自限性疾病,即使不进行相应抗病毒治疗也有可能治愈,那么就减弱了小样本研究的说服力。
原北京协和医学院教授、从事免疫治疗药物研发的王晨光博士认为,行政手段干预临床研究项目上马的做法并不乐观。毕竟目前国家政策是大力推进中医药发展,管理部门可能对延缓某些中医药项目畏手畏脚。
需要强调现代医学标准

美国国立卫生研究院下属国家过敏症和传染病研究所主任安东尼·福奇(Anthony Fauci)称,美国迫切需要一种安全有效的新冠肺炎疗法,而随机的安慰剂对照临床试验是判断试验性疗法的黄金标准。
福奇提到的金标准是现代医学的内容。与传统医学的不同处是,循证医学并不依赖于经验主义或过往案例,随机对照试验才是循证医学证据的主要来源。比如北京大学第一医院呼吸和危重症医学科主任王广发口中对其有效的“洛匹那韦利托那韦片”,该药曾在国家卫生健康委员会颁布的《新型冠状病毒肺炎诊疗方案(试行第二版)》中被推荐试用。然而在上海市公共卫生临床中心团队发表于《中华传染病杂志》的研究中未发现该药能改善症状。
中国循证医学中心创建主任李幼平教授在2014年《世界卫生组织简报》中表示,许多人不了解循证医学是什么,质疑循证医学对中国有什么用。中国生产的有一些临床证据还不符合国际标准,主要因为没有足够的合格研究者,对临床试验的监管也不够。李幼平于2007年领导创建了中国临床试验注册中心,成为世卫组织国际临床试验注册平台的一级注册机构。
最近一篇刷屏的自媒体文章《循证的崩溃》称,循证医学在中国本来就虚弱得可怜,在暴虐的新冠病毒面前,已经濒于全面崩溃。
众多临床试验中,不管是化学药物还是传统药物,或者是恢复期患者的血浆疗法,大都没有做到严格遵守医学原则。《中华流行病学杂志》文章也指出,因为 SARS时期我们有了足够的教训,不能再犯这类错误。治疗无效不等于没有副作用,尤其是在这个时候,不允许将无效药物的风险转嫁给患者。
瑞德西韦的研究是极少数有望坚持现代医学的项目之一。需要说明的是,曹彬的瑞德西韦研究是在美国临床试验数据库(ClinicalTrials.gov)注册的。
一位医学权威专家在接受 DeepTech采访时指出,曹彬的瑞德西韦试验是一个举世瞩目的临床研究,建议他完全按照预先设计的方案,所有的入组条件不能改变,即使最终的研究结果说服力不够,但至少其研究结果可以让后来者作为原始依据进行二次研究。
该专家表示,如果说非要改变入组条件,就要将符合严格标准的分为一组,放宽标准的分为一组,这样也至少能够尽量避免患者入组标准前后不一带来的影响。
王晨光也指出,此次疫情中大量患者本来是极为珍贵的医疗资源,如果没有利用得当,那么就白白浪费了医学资源,辜负了疫情受害者的牺牲,并且这些不当作为可能在下一次疫情来袭时再度上演,那才是一个最糟糕的结局。
附件:从1月23日到2月27日,在中国临床试验注册中心新型冠状病毒肺炎临床研究索引中已经有271个结果。(上下滑动可看全部内容)



















