联邦食品暨药物管理局(FDA)8日批准了全球第一种采用Crispr基因编辑技术开发而成的药物;这项名为Casgevy的新疗法,将用来治疗镰状细胞疾病(sickle-cell disease,SCD)患者。
华尔街日报形容FDA的决定具里程碑意义,让“基因编辑革命从实验室走向市场”。
基因革命 从实验室走向市场
因协助发明Crispr技术获得2020年诺贝尔奖的珍妮佛·道纳(Jennifer Doudna)指出,该疗法获批准“几乎改变了我们定义药物的方式”,并“彰显基因疗法前景:透过有针对性地改变人类DNA,从源头治疗疾病。”
FDA历史性地批准Casgevy疗法的同一天,也批准了与该疗法竞争的基因替代疗法Lyfgenia,该疗法也用于治疗治疗12岁以上的镰状细胞疾病患者。
Casgevy疗法是由福泰制药(Vertex Pharmaceuticals)和瑞士基因编辑公司Crispr Therapeutics共同开发;这种新型药物强大到可以关闭或替换基因,解决过去长期困扰医生和研究人员的疾病和问题。目前有数家公司都在开发Crispr技术疗法,用以治疗心脏病、癌症和罕见遗传性疾病等。
美国有10万人患镰状细胞疾病
镰状细胞疾病是遗传性基因突变引起,会导致血液中携带氧气的血红素或血红蛋白(hemoglobin)出现功能障碍。非裔患者较多,会导致剧烈疼痛、器官损伤和早逝。现有少数可用疗法有助治疗并发症,但不能治疗潜在病源。美国约有10万名患者,全球患者逾2000万人。
Casgevy疗法与其他正在开发的Crispr药物不同,它在实验室进行基因编辑,而不是在患者体内对患者细胞进行基因编辑。它生出一种会在子宫内产生的胎儿血红蛋白,功能性地替代因镰状细胞疾病导致的畸形成人血红蛋白。
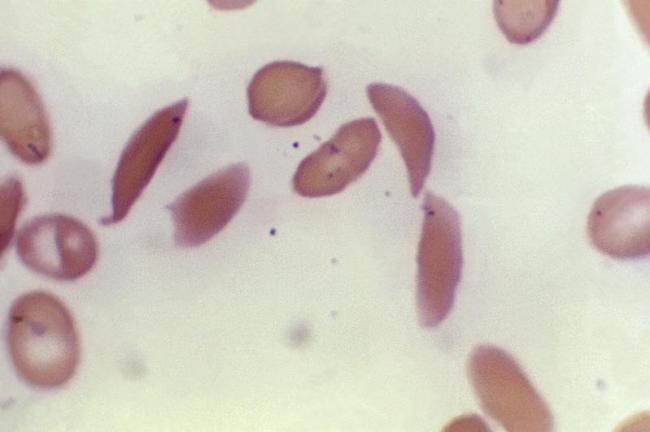
FDA核准全世界首个基因编辑疗法,治疗镰状细胞疾病,这对未来一些遗传疾病的治疗带来很大希望。该疾病会导致血液中携带氧气的血红素或血红蛋白出现功能障碍,图为患者功能受损的血红素。
由于Casgevy疗法是在体外编辑细胞,有助确保治疗不会意外改变与疾病无关的其他基因;但患者须接受数日的高剂量化疗,以便为修改后的细胞腾出空间。
Casgevy疗法昂贵 定价220万元
不过,华尔街日报指出,Casgevy疗法的使用至少初期可能会受限,因为若Casgevy价格太高,部分健保计划可能不会承保;有些患者也可能会因为须住院数周接受治疗或因化疗通常会导致不孕,却步不前。
生产Lyfgenia的蓝鸟生物公司(Bluebird Bio)将药价定为310万元,生产和销售Casgevy疗法的福泰制药则将Casgevy疗法定价下调至220万元。
旧金山加州大学儿科教授兼镰状细胞研究员沃尔特斯(Mark Walters)表示,“这项疗法有可能带来变革,但也会非常昂贵。”

FDA8日核准全世界第一个利用基因编辑治疗遗传疾病的药物。
福泰制药科学长奥夏勒(David Altshuler)表示,尽管施药过程密集复杂,但“相信很多人会觉得很值得”。福泰制药将很快公布药价,预计此法将被全美2万名严重镰状细胞疾病患者使用。



















